科普漫画《农小药和桃小果》
2023-09-29
发布时间:2024-09-09 来源:《农药科学与管理》2024年第8期 作者:作者:宋俊华,叶贵标 浏览次数:1255
《农药科学与管理》2024年第8期
2024-09-09
![]() 1255
1255
联合国粮食与农业组织(fao)和世界卫生组织(who)倡导通过健全的生命周期管理减少农药使用风险,推荐将有害生物综合治理(ipm)和病媒生物综合管理(ivm)作为防治有害生物的首选方法,鼓励各国农药管理部门执行《fao/who国际农药管理行为守则》。产品质量控制是农药全生命周期管理中至关重要的一环,是促进包括微生物农药在内的生物农药使用,实现ipm和ivm管理目标的重要基础。为协助各国做好微生物农药质量管理,在全球范围内协调微生物农药产品标准的制定和使用,2024年fao和who首次联合发布第一版《fao/who微生物农药标准制定和使用手册》(以下简称《微生物农药标准手册》),本文对其进行了系统介绍,供我国农药生产、使用和管理等相关单位参考。
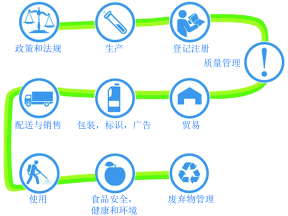
图1 fao农药全生命周期管理
1 背景
在fao和who 现已发布的300多种(有效成分计)农药产品标准中,仅含有4种生物农药标准(表1),与其倡导的ipm/ivm管理理念和对生物农药的需求相比都存在很大差距。2017年,在参考《oecd微生物农药国家资料评审报告指南》(经济合作与发展组织oecd,2006)等oecd相关生物农药导则的基础上,fao和who联合制定并发布了《fao/who植保和卫生用微生物、植物源和信息素类产品登记指南》。同时考虑到微生物农药与化学农药在有效成分特性及产品质量控制领域的巨大差异,将原《fao/who农药产品标准制定和使用手册》(2016,第一版第3次修订)(以下简称为原《手册》)分拆为2个部分,分别为2022年发布的《fao/who化学农药产品标准制定和使用手册》(第二版)以及2024年发布的第一版《微生物农药标准手册》,后者取代原《手册》中的第9章—微生物农药产品标准。两部手册分别针对化学农药和微生物农药标准制定,两者相互关联,在程序等通用章节方面具有相似性,但在资料要求和判定标准等部分内容上存在明显差异。
2 《微生物农药标准手册》介绍
2.1 基本情况及特点 《微生物农药标准手册》将微生物母药(mpca)定义为:具有有害生物防控作用的微生物(原生动物、真菌、细菌、病毒或其他显微镜级别的自我复制有机体)及其相关代谢物。微生物活性成分包含微生物活体和(或)非活体,同时包括细胞增殖(生长)过程中产生的相关代谢物或毒素以及生长介质中产生的、没有被人为改变过的物质;微生物农药制剂(mpcp)定义为:含有已登记或拥有使用说明标签的 mpca 的产品。上述定义与oecd和fao/who参考指南中的定义一致。

在原《手册》第9章的基础上,《微生物农药标准手册》增加了微生物农药品种,其中明确涵盖的微生物包括细菌、真菌和病毒,但病毒目前仅重点关注杆状病毒(baculovirus),不包含转基因生物、rna 干扰技术类产品和大的生物体(macro-organism)等。增加了剂型规范模板,包含母药在内的7种微生物农药剂型,包括母药(tk)、颗粒剂(gr)、可湿性粉剂(wp)、水分散粒剂(wg)、可分散片剂(wt)、悬浮剂(sc)和种子处理悬浮剂(fs)。另外根据上述oecd指南和fao/who指南相关内容,结合标准制定的特点,细化了申请资料要求。
根据《微生物农药标准手册》,申请微生物农药fao/who标准,总体呈现以下几个特点:1.视产品具体情况,可引用公开发布的信息作为资料要求的一部分,或申请报告豁免;2.不需要制定有效成分cipac(国际农药分析协作委员会)分析方法,可使用实验室内自行验证或经过同行比对(peer validation)验证过的方法,无需对方法进行大范围协同验证;3.试验报告不一定由oecd glp实验室出具;4.目前尚未开展微生物农药的相同产品认定评审,后期可能会考虑主要针对苏云金杆菌的母药等同性认定。
2.2 微生物农药母药标准申请 对于微生物母药标准申请,资料要求主要包括以下几个方面内容:微生物定性、母药及有效成分组成、定量分析方法、生产工艺以及毒理和环境毒理数据等。申请fao/who微生物农药产品标准,微生物有效成分要求定性到菌株级别,并提交国际认可的菌株保存中心的菌株样品代号,以证明其安全性,同时识别潜在的不良影响。目前全球共有48家国际培养物保藏机构(ida),分布在26个国家或者地区,国内有3家获得布达佩斯条约国际保藏中心资格的菌种保存中心,分别为中国微生物菌种保藏管理委员会普通微生物中心(cgmcc)、中国典型培养物中心(cctcc)和广东省微生物菌种保藏中心(gdmcc)。通常情况下,应使用最方便、成熟的微生物分析技术对微生物有效成分进行明确识别。如需使用更先进的、基于分子识别的鉴别技术,如通过pcr进行dna扩增以进行后续测序/杂交等方法进行的基因型鉴定,则必须为基因(或dna/rna的一部分)和引物的选择提供解释和说明。
微生物母药中有效成分含量需以g/kg、g/l、菌落形成单位(cfu)、生物效价单位或其他适当的以单位重量或体积计的微生物单位表示,需要注意的是,微生物农药含量应以活性微生物而不是总微生物的含量计。除有效成分外,微生物母药中还可能含有培养基及微生物污染物和次生化合物等,视需要也需提供相关含量或限量信息。上述信息需提供3~5批次母药的质量控制数据(标准全项检测报告)及储存稳定性数据予以佐证,并与生产工艺中反映出的信息一致。
因cipac不制定和发布微生物农药有效成分分析方法,按照《微生物农药标准手册》的要求,微生物农药母药及相关杂质的定量方法需进行实验室内确认以及实验室间的同行验证,并提交相关验证报告和数据。
与化学农药不同,微生物农药标准中的相关杂质来源分为以下3类:微生物污染物、化学杂质(来自生产过程中)和次生化合物。对于微生物农药中微生物污染物限量的管理,国际社会中普遍认可的准则为《oecd关于微生物有害生物防治产品中微生物污染物限量的文件》。该文件在广泛借鉴美国、加拿大、欧盟以及各类国际组织制定的食品和饮用水中微生物限量准则的基础上,规定了微生物农药登记管理中需要进行筛查的微生物污染物清单及限量。筛查对象主要包括人类致病菌,并不涵盖植物致病菌。致病菌依据其危害主要分为四类,包括严重危害、中等危害且有广泛传播的潜在性、中等危害且有有限传播的潜在性和其他需要关注的致病菌。具体筛查要求视产品的生产工艺和质量控制情况做最后确定。与行业一般推荐采用0.1%的感染繁殖体数量作为杂菌的限量指标不同,文件对杂菌限量采用了食品和饮用水中的限量值,因微生物在人体和环境中的运行机制存在很大不同,部分对于微生物农药来说过于严格。我国目前还未要求微生物产品登记时进行致病菌的筛查,仅要求检测广义的杂菌率指标并提供限值。




2.3 微生物农药制剂标准申请 传统化学农药制剂产品申请fao/who产品标准,在所使用的原药经过fao/who评价的前提下,除通用信息外,制剂产品仅需要提供批次全项检测数据即可(缓释剂型和长效蚊帐等who剂型产品除外)。相较之下,微生物农药制剂申请fao标准需要提供的资料较多,除批次检测数据外,还需提供产品组成、理化性质、常储数据以及6项急性毒性数据和部分生态毒理数据(如已对微生物农药母药的危害和暴露进行了评估,对于微生物农药制剂,可减免该部分资料)。
因大多数微生物对高温敏感,适用于常规化学农药的cipac mt 46.4热贮稳定性试验可能不适用于微生物农药,因此《微生物农药标准手册》要求微生物农药热储后仅对相关理化指标进行检测,而不检测有效成分含量。另外,对在低温贮存时可能影响有效成分含量的固体制剂,也需要进行低温稳定性检测,以确定温度对有效成分含量的影响。对于微生物农药制剂标准中的部分质量控制指标,依据产品特性,可考虑制定更加宽松的限量,如自动分散性和悬浮率可允许<60%,湿筛指标可允许>2%等。


3 我国企业申请fao/who微生物农药标准面临的机遇及挑战
在全球各国不断提高化学农药准入门槛以及消费者对食品和环境安全日益关注的大背景下,fao/who等国际组织以及各国农药管理部门均鼓励包括微生物农药在内的生物农药发展,包括缩短登记评审时间和降低评审费用等。从fao/who首家产品标准角度,与化学农药相比,申请微生物农药标准所需报告无严格glp要求,费用远低于化学农药;有效成分分析方法也无需为cipac方法,且在合理解释的前提下,可提供大量查阅资料用于代替试验报告,为我国企业申请制定fao/who微生物农药标准创造了良好的外部条件。另外,中国农业农村部发布《到2025年化学农药减量化行动方案》以及《“十四五”全国农药产业发展规划》,旨在实施病虫害绿色防控和农药减量增效行动,在降低化学农药使用的同时,鼓励促进生物农药使用,对生物农药登记实施“绿色通道”政策,而且我国是除了美国以外生物农药登记品种最为丰富的国家,已登记生物农药有效成分152个、产品2 000余个,生物农药特别是微生物农药管理制度相对规范,已发布微生物农药产品质量相关标准50多项,微生物农药的毒理学试验准则5项、微生物农药环境安全试验类准则9项以及部分微生物农药生产规程类标准,以上为我国企业申请制定fao/who微生物农药标准提供了坚实的政策和尊龙凯时平台入口的技术支持。
尽管如此,中国企业申请制定fao/who微生物农药标准仍存在诸多挑战。首先,现行oecd和cipac等部分国际通行配套试验准则并不完全适用于微生物农药,微生物农药各项管理及试验准则均有待制定或规范。如因oecd皮肤致敏性导则适用性的问题,欧盟默认所有微生物农药均为皮肤致敏性物质,除非另外提供证据说明。用于建立微生物有效成分含量分析方法的实验室内及实验室间确认导则均缺乏,《微生物农药标准手册》也未对此进行明确。其次,部分微生物农药fao/who标准所需资料在我国微生物农药登记时并未要求提供,如对生产用主菌种的要求、对单个杂菌(微生物污染物)的定性定量要求;或部分要求不同,如分析方法的实验室内或实验室间验证等,都给我国企业申请制定标准增加了难度;另外,我国微生物生产企业相较于化学农药生产企业,总体规模较小,实力相对较弱,我国企业已成功申请化学农药fao/who产品标准40多个,但至今在微生物农药尚未有突破。最后,企业在微生物农药开发时往往注重药效,而产品鉴别不清影响安全性的确认;以及缺乏经验丰富的检测实验室等,都给微生物农药标准申请带来了一定的挑战。
建议我国生物农药生产企业可充分发挥现有优势,熟悉标准制定相关要求,加大专业人才的培养力度,牵头制定部分通用类或产品类国际标准,在填补国际空白的同时增强我国在生物农药管理领域的话语权,加快我国生物农药走出去的步伐。
 回到顶部
回到顶部